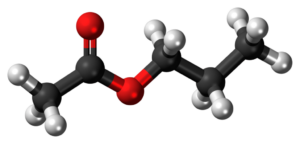
Este phenol là một loại hợp chất hữu cơ quan trọng, được tạo thành từ phản ứng giữa phenol và axit cacboxylic. Những hợp chất este phenol có nhiều ứng dụng hữu ích trong các lĩnh vực như dược phẩm, hóa mỹ phẩm, sản xuất nhựa và hóa chất. Việc hiểu rõ cách tính toán và giải các bài tập về este phenol và NaOH là rất cần thiết cho những ai đang học hóa học, đặc biệt là ở cấp độ đại học.
Trong bài viết này, Học văn vui vẻ sẽ cung cấp cho bạn một hướng dẫn chi tiết về cách giải các bài tập liên quan đến este phenol và NaOH. Chúng tôi sẽ đi qua các bước cơ bản, cung cấp ví dụ minh họa và chia sẻ một số mẹo hữu ích để giúp bạn nắm vững kiến thức và giải quyết thành thạo những bài tập này.

Tổng Quan Về Este Phenol và NaOH
Este phenol là một loại hợp chất hữu cơ có công thức chung là R-COO-Ph, trong đó R là một gốc alkyl hoặc aryl, và Ph là gốc phenyl. Các este phenol được tạo thành từ phản ứng của phenol với axit cacboxylic hoặc anhydrit axit.
Natri hydroxid (NaOH) là một hợp chất vô cơ, còn được gọi là natri kiềm hoặc thuỷ tinh ăn. NaOH là một chất kiềm mạnh, thường được sử dụng trong nhiều ứng dụng công nghiệp và hóa học, như sản xuất xà phòng, giấy, thuốc nhuộm, và làm chất tẩy rửa.
Trong các bài tập liên quan đến este phenol và NaOH, chúng ta thường gặp các chủ đề như:
- Tính toán phản ứng este hoá giữa phenol và axit cacboxylic.
- Xác định sản phẩm của phản ứng este hoá và tính toán hiệu suất phản ứng.
- Giải quyết các vấn đề liên quan đến NaOH, chẳng hạn như tính toán nồng độ, pH, và khối lượng/thể tích.
- Phân tích các tính chất của este phenol và NaOH, như nhiệt độ sôi, điểm nóng chảy, tính chất hóa học, v.v.
Để giải quyết thành thạo những bài tập này, chúng ta cần hiểu rõ về cấu trúc, tính chất và các phản ứng liên quan của este phenol và NaOH.
Cách Giải Bài Tập Về Este Phenol và NaOH
Dưới đây là một hướng dẫn chi tiết về cách giải các bài tập liên quan đến este phenol và NaOH:
1. Xác Định Phản Ứng Este Hoá
Trong bài tập về este phenol, trước tiên chúng ta cần xác định phản ứng este hoá giữa phenol và axit cacboxylic. Phản ứng este hoá có thể được viết dưới dạng phương trình hoá học như sau:
Phenol + Axit cacboxylic → Este phenol + Nước
Ví dụ: Phenol + Axit acetic → Acetate phenol + Nước
Để hoàn thành bài tập, chúng ta cần xác định các sản phẩm của phản ứng este hoá và tính toán hiệu suất phản ứng.
2. Tính Toán Hiệu Suất Phản Ứng
Để tính toán hiệu suất phản ứng este hoá, chúng ta có thể sử dụng công thức sau:
Hiệu suất phản ứng (%) = (Khối lượng sản phẩm este phenol / Khối lượng phenol ban đầu) x 100
Ví dụ: Nếu chúng ta có 10 gam phenol và thu được 15 gam este phenol, thì hiệu suất phản ứng sẽ là:
Hiệu suất phản ứng (%) = (15 g / 10 g) x 100 = 150%
Lưu ý rằng hiệu suất phản ứng có thể vượt quá 100% nếu có sự chuyển dịch cân bằng hoặc phản ứng phụ khác xảy ra.
3. Tính Toán Liên Quan Đến NaOH
Trong một số bài tập, chúng ta cũng cần giải quyết các vấn đề liên quan đến NaOH, chẳng hạn như tính toán nồng độ, pH, khối lượng hoặc thể tích.
Ví dụ: Nếu chúng ta có 50 ml dung dịch NaOH 0,1 M, hãy tính khối lượng NaOH trong dung dịch.
Để giải quyết vấn đề này, chúng ta sử dụng công thức:
Khối lượng NaOH (g) = Nồng độ (M) x Thể tích (L) x Khối lượng mol (g/mol)
Với NaOH, khối lượng mol là 40 g/mol.
Thế vào công thức:
Khối lượng NaOH (g) = 0,1 M x 0,05 L x 40 g/mol = 0,2 g
Vì vậy, trong 50 ml dung dịch NaOH 0,1 M, có 0,2 g NaOH.
Phân Tích Tính Chất của Este Phenol và NaOH
Trong một số bài tập, chúng ta cần phân tích các tính chất của este phenol và NaOH, chẳng hạn như nhiệt độ sôi, điểm nóng chảy, tính chất hóa học, v.v.
Ví dụ: So sánh nhiệt độ sôi của este phenol và este alkyl (ester thông thường).
Để giải quyết vấn đề này, chúng ta cần hiểu rằng este phenol có nhiệt độ sôi cao hơn este alkyl do sự tương tác giữa gốc phenyl và liên kết ester. Sự tương tác này làm tăng lực hút giữa các phân tử, dẫn đến nhiệt độ sôi cao hơn.
Tương tự, chúng ta có thể phân tích các tính chất khác của este phenol và NaOH dựa trên cấu trúc và tính chất hóa học của chúng.
Ví Dụ Minh Họa
Hãy giải quyết bài tập sau:
Phenol phản ứng với axit acetic để tạo thành este phenyl axetat. Tính hiệu suất phản ứng nếu chúng ta bắt đầu với 12 gam phenol và thu được 18 gam este phenyl axetat.
Giải:
- Xác định phản ứng este hoá: Phenol + Axit acetic → Este phenyl axetat + Nước
- Tính hiệu suất phản ứng: Hiệu suất phản ứng (%) = (Khối lượng sản phẩm este phenyl axetat / Khối lượng phenol ban đầu) x 100 Hiệu suất phản ứng (%) = (18 g / 12 g) x 100 = 150%
Như vậy, với 12 gam phenol ban đầu và thu được 18 gam este phenyl axetat, hiệu suất phản ứng este hoá là 150%.
Mẹo Giải Bài Tập

Dưới đây là một số mẹo hữu ích để giải các bài tập về este phenol và NaOH:
- Nhớ các công thức cơ bản: Hiệu suất phản ứng, tính toán nồng độ, khối lượng, thể tích, pH, v.v.
- Đọc kỹ câu hỏi để xác định các thông tin quan trọng cần tính toán.
- Vẽ sơ đồ phản ứng hoặc sơ đồ cấu trúc để hình dung rõ ràng về quá trình.
- Kiểm tra đơn vị và đảm bảo các đơn vị được sử dụng đúng cách.
- Thực hành nhiều ví dụ và bài tập để nắm vững kiến thức.
- Tham khảo tài liệu tham khảo và hướng dẫn từ giáo viên nếu cần.
Kết Luận
Trong bài viết này, chúng tôi đã cung cấp cho bạn một hướng dẫn chi tiết về cách giải các bài tập liên quan đến este phenol và NaOH. Chúng tôi đã đi qua các bước cơ bản, bao gồm xác định phản ứng este hoá, tính toán hiệu suất phản ứng, giải quyết các vấn đề liên quan đến NaOH, và phân tích tính chất của các hợp chất.
Bằng cách áp dụng các kỹ thuật và mẹo được chia sẻ trong bài viết này, bạn sẽ có thể giải quyết thành thạo các bài tập về este phenol và NaOH. Hãy thực hành thường xuyên, tham khảo tài liệu tham khảo, và không ngần ngại hỏi giáo viên nếu bạn gặp bất kỳ khó khăn nào.
Học văn vui vẻ chúc bạn học tập và làm việc hiệu quả!